问题分析: 1906年Janeway使狗的一侧肾动脉缩窄后产生高血压持续105天,但未作进一步研究;直到1934年Goldblatt实验造成肾缺血性高血压的动物模型后,才重新引起人们的重视,从而奠定了肾血管性高血压的理论基础。
肾动脉缩窄发生高血压的机理尚未完全瞭解。一般认为肾血流量的减少导致肾缺是一个促进条件,但有人在狗肾动脉缩窄的前后,用肾血流量直接测定法发现在轻度或??肾动脉缩窄引起的高血压时,肾血流量的减少仅为暂时性的。随着侧支循环的建立,肾血流量就可回到正常范围。有人使动物呼吸少氧的气体或用静脉血灌注肾脏也不产生高血压。因此,肾缺血、缺氧虽是促成肾血管性高血压的因素,但学有其他的条件存在。
有关肾血管性高血压的发病原理,文献中有多种论点。目前较为普遍公认的主要有下列三种:
一、肾脏的升压体系—肾素、血管紧张素、醛固酮体系(renin-angiotensin-aldosterone system),即RAA体系肾素是一种蛋白水解酶,具有不耐热和不可透析的特性。肾素本身不是加压素,必须与肝内产生的α2球蛋白(又称肾素激活素或高压素或高压素原,其中包含一种能被肾素作用的底物)相结合才发生效用。当肾素作用于肾素底物(renin substrate)的分子结构,使在第10及第11亮氨酸连接处断裂,释出十肽成为血管紧张素Ⅰ(angiotensin Ⅰ,AⅠ)。血管紧张素Ⅰ亦无升压作用。当它流径各脏器血管床时,特别在肺循环被转化酶在其分子结构第8~9位之间断裂,释出八肽,成为血管紧张素Ⅱ(AⅡ)。它是一种强有力的血管收缩剂。近来提出从血管紧张素Ⅱ再由氨基转肽酶去除第一位氨基酸释出一种七肽,称为血管紧张素(AⅢ)。此物刺激醛固酮的分泌作用比血管紧张素Ⅱ强数倍。血管紧张素Ⅱ~Ⅲ的作用:①直接使血管收缩;②经交感神经系统而间接收缩血管;③收缩输出小动脉而输入小动脉不收缩,从而增加肾小球压力,减少钠排出;④刺激肾上腺皮质分泌醛固酮。血管紧张素Ⅱ和Ⅲ在血循环中的半衰期仅数分钟,降解后形成小分子的无活性产物氨基酸,二肽、三肽。因此,高血压的维持还要依靠肾上腺素和醛固酮的作用。
肾脏除产生肾素外,也产生高血压蛋白酶。后者有分解血管紧张素的作用。在正常情况下,两者保持平衡状态不引起高血压。如肾缺血,缺氧时,肾素的分泌增多,从而破坏了正常平衡,产生过多的血管紧张素而引起高血压。
实验证明,肾脏对醛固酮的分泌能起作用,血管紧张素Ⅱ和Ⅲ均可刺激醛固的分泌。这说明血管紧张素Ⅱ和Ⅲ所产生的高血压,一方面是使细动脉收缩,增加周围阻力;另一方面是通过醛固酮分泌的增加,促进钠和水的潴留,使细胞外液的容量增加,故而形成肾素-血管紧张素-醛固酮体系。
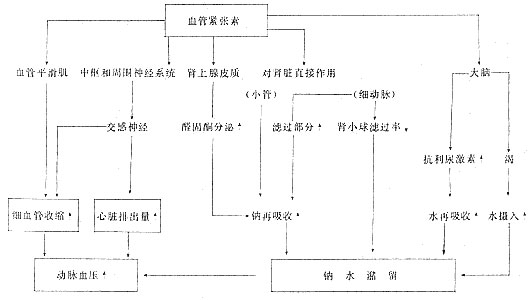
Vander(1984)对肾素-血管紧张素-醛固酮体系的作用了全面的阐明(图9)。
 二、肾脏调节高血压物质的体系 近期内,许多实验证明除上述肾素-血管紧张素-醛固酮体系外,尚发现有另一种调节血压的体系,即激肽释放酶-激肽-前列腺素体系(kallikreinkinin-prostaglandin system,KKP体系)。
1.肾脏的激肽释放酶-激肽系统(renal kallikrein-kinin system) 激肽系由肝脏的激肽原受到肾脏产生的激肽释放酶作用转变而来。肾脏的激肽释放酶90%以上分布于皮质,髓质占4.5%和乳头占4.1%,皮质中肾小球所含激肽的活性酶只占1.5%,而主要生成部位可能在肾小球旁体。激肽释放酶的活性越高,催化激肽原水解、生成激肽越多。另外,肾脏能分泌激肽水解酶,可以破坏所产生的激肽。
目前认为肾激肽有下列作用:①促进小动脉舒张,使外周血管阻力下降;②肾内小动脉舒张,肾血流量增加,改善肾皮质缺血;③促进钠、水的排出,水的排出比钠为多,故尿渗压下降。水、钠排出增加导致血浆容量减少,使血液红细胞压积及血浆总蛋白浓度增加;④由于血管外周围阻力下降及循环血量减少,可使血压下降,故有抗高血压的作用。
以上作用主要通过激肽促进前列腺素的生成所引起的,但其中也有一部分是激肽的直接作用。
2.肾脏的前列激素 目前已检测出的前列腺素有多种,而在肾髓质中可以分离出来的前列腺素三种,即PGE2、PGA2、PGF2α。前列腺素在肾皮质内含量很低,在髓质中以乳头的含量较高。在肾内PGE2的量较少,主要是PGA2和PGF2α。一般不能在细胞内贮存,一旦合成后即释放出来,通过肾内循环被运转到皮质发挥生理效益,另一部分PGE2、PGF2α经肾静脉进入体循环被肺组织破坏,而PGA2可以在体循环中存在。
肾前列腺素的作用:①肾动脉内灌液PGE2可引起局部血管扩张,使肾血流量增加;②前列腺素还可使肾血流重新分配,即使髓质血流下降和使皮内层血流量增加;③PGE2和PGA2可引起肾入球动脉舒张,使近曲小管周围毛细血管压力上升,因而使近曲小管对水和盐的重吸收能力降低。PGA2、PGE2可抑制肾小管细胞膜上的Na+-K--ATP酶的活生,使细胞内Na+不易运转至肾小管周围液体中,影响了肾小管对钠和水的重吸收,从而出现利尿作用。PGE2还能抑制抗利尿激素而使尿量增加,促进钠、钾、水的排出。肾前列腺素还有拮抗儿茶酚胺的使用,但不能抑制儿茶酚胺的分泌。故腺舦-前列腺素体系具有调整肾素增高的作用。这是由于血管紧张素促使醛固酮分泌增高,后者可使前列腺素释放酶的分泌增加,从而加速前列腺素PGA2、PGE2的合成。
三、去肾性高血压(renoprival hypertension)去肾性高血压是指肾组织没有功能所产生的高血压而言,也可称为肾缺如性高血压或肾切除后高血压。肾脏除有抗高血压物质外,尚有调节体液、电解质的功能和排出体内升压因素的作用。临床所见高血压病人比正常人排出较多的水和钠,而水的排出量又相对较多,因而体内钠的比例反有增高。在另一方面,高血压的发生,一般见于体内水分增加,失水后可使血压下降,大量输液后血压升高,在尿毒症高血压病人中更为明显。这类病人对钠和水的潴留较为敏感,动物实验也证实类似现象。肾组织大量减少可使动物对高盐饮食很敏感;双肾切除后高盐摄入可以引起去肾性高血压。因此,肾组织完全丧失功能如同双肾切除一样,所发生的高血压显著与体液和钠盐平衡失调有关。此外,体内的升压物质因去肾后不能排出,积聚而使血压升高。
结合上述三种论点,对临床所见肾血管性高血压病例中出现三种类型的周围血管液肾素值问题可阐明如下。
1.高肾素型高血压即血管收缩性高血压。在动物实验中可以造成这样一种模型。缩窄一侧肾动脉,另一侧保持正常。肾动脉狭窄后肾内血供减少和肾内压降低促使肾素分泌增多,导致血管紧张素升高而产生高血压。对侧健肾因受高血压的冲击使其肾素分泌下降。患肾肾素的增设值超过健肾肾素的减少量,结果血浆内肾素值高于正常,形成高肾素型高血压。在治疗上可用抗肾素的药物。
2.低肾素型高血压即血容量性高血压。这种动物实验模型是缩窄一侧肾动物?K切除对侧肾脏。由于只有孤立病肾,钠和水排出降低,钠潴留又使细胞外液量亦即血容量扩张,从而产生高血压。肾内压?K不低于原有水平,因之肾素分泌也不增加。在血容量增加的条件下,血浆内肾素值则相应地低于正常,形成低肾素型高血压。在治疗上不用抗肾素的药物,而用利尿排钠的药物。
3.正常肾素型高血压即混合型高血压。原发性高血压中常见。这类病变的肾脏兼有排钠障碍和肾素分泌增加,即一方面血容量增加,一方面小动脉收缩加强,两者均可导致血压升高。血压升高和血容量增加又可抑制肾素分泌,最后达到平衡,即肾素张素、醛固酮的分泌均在正常范围之内。在治疗上需联合应用利尿排钠剂和抗肾素的药物。
二、肾脏调节高血压物质的体系 近期内,许多实验证明除上述肾素-血管紧张素-醛固酮体系外,尚发现有另一种调节血压的体系,即激肽释放酶-激肽-前列腺素体系(kallikreinkinin-prostaglandin system,KKP体系)。
1.肾脏的激肽释放酶-激肽系统(renal kallikrein-kinin system) 激肽系由肝脏的激肽原受到肾脏产生的激肽释放酶作用转变而来。肾脏的激肽释放酶90%以上分布于皮质,髓质占4.5%和乳头占4.1%,皮质中肾小球所含激肽的活性酶只占1.5%,而主要生成部位可能在肾小球旁体。激肽释放酶的活性越高,催化激肽原水解、生成激肽越多。另外,肾脏能分泌激肽水解酶,可以破坏所产生的激肽。
目前认为肾激肽有下列作用:①促进小动脉舒张,使外周血管阻力下降;②肾内小动脉舒张,肾血流量增加,改善肾皮质缺血;③促进钠、水的排出,水的排出比钠为多,故尿渗压下降。水、钠排出增加导致血浆容量减少,使血液红细胞压积及血浆总蛋白浓度增加;④由于血管外周围阻力下降及循环血量减少,可使血压下降,故有抗高血压的作用。
以上作用主要通过激肽促进前列腺素的生成所引起的,但其中也有一部分是激肽的直接作用。
2.肾脏的前列激素 目前已检测出的前列腺素有多种,而在肾髓质中可以分离出来的前列腺素三种,即PGE2、PGA2、PGF2α。前列腺素在肾皮质内含量很低,在髓质中以乳头的含量较高。在肾内PGE2的量较少,主要是PGA2和PGF2α。一般不能在细胞内贮存,一旦合成后即释放出来,通过肾内循环被运转到皮质发挥生理效益,另一部分PGE2、PGF2α经肾静脉进入体循环被肺组织破坏,而PGA2可以在体循环中存在。
肾前列腺素的作用:①肾动脉内灌液PGE2可引起局部血管扩张,使肾血流量增加;②前列腺素还可使肾血流重新分配,即使髓质血流下降和使皮内层血流量增加;③PGE2和PGA2可引起肾入球动脉舒张,使近曲小管周围毛细血管压力上升,因而使近曲小管对水和盐的重吸收能力降低。PGA2、PGE2可抑制肾小管细胞膜上的Na+-K--ATP酶的活生,使细胞内Na+不易运转至肾小管周围液体中,影响了肾小管对钠和水的重吸收,从而出现利尿作用。PGE2还能抑制抗利尿激素而使尿量增加,促进钠、钾、水的排出。肾前列腺素还有拮抗儿茶酚胺的使用,但不能抑制儿茶酚胺的分泌。故腺舦-前列腺素体系具有调整肾素增高的作用。这是由于血管紧张素促使醛固酮分泌增高,后者可使前列腺素释放酶的分泌增加,从而加速前列腺素PGA2、PGE2的合成。
三、去肾性高血压(renoprival hypertension)去肾性高血压是指肾组织没有功能所产生的高血压而言,也可称为肾缺如性高血压或肾切除后高血压。肾脏除有抗高血压物质外,尚有调节体液、电解质的功能和排出体内升压因素的作用。临床所见高血压病人比正常人排出较多的水和钠,而水的排出量又相对较多,因而体内钠的比例反有增高。在另一方面,高血压的发生,一般见于体内水分增加,失水后可使血压下降,大量输液后血压升高,在尿毒症高血压病人中更为明显。这类病人对钠和水的潴留较为敏感,动物实验也证实类似现象。肾组织大量减少可使动物对高盐饮食很敏感;双肾切除后高盐摄入可以引起去肾性高血压。因此,肾组织完全丧失功能如同双肾切除一样,所发生的高血压显著与体液和钠盐平衡失调有关。此外,体内的升压物质因去肾后不能排出,积聚而使血压升高。
结合上述三种论点,对临床所见肾血管性高血压病例中出现三种类型的周围血管液肾素值问题可阐明如下。
1.高肾素型高血压即血管收缩性高血压。在动物实验中可以造成这样一种模型。缩窄一侧肾动脉,另一侧保持正常。肾动脉狭窄后肾内血供减少和肾内压降低促使肾素分泌增多,导致血管紧张素升高而产生高血压。对侧健肾因受高血压的冲击使其肾素分泌下降。患肾肾素的增设值超过健肾肾素的减少量,结果血浆内肾素值高于正常,形成高肾素型高血压。在治疗上可用抗肾素的药物。
2.低肾素型高血压即血容量性高血压。这种动物实验模型是缩窄一侧肾动物?K切除对侧肾脏。由于只有孤立病肾,钠和水排出降低,钠潴留又使细胞外液量亦即血容量扩张,从而产生高血压。肾内压?K不低于原有水平,因之肾素分泌也不增加。在血容量增加的条件下,血浆内肾素值则相应地低于正常,形成低肾素型高血压。在治疗上不用抗肾素的药物,而用利尿排钠的药物。
3.正常肾素型高血压即混合型高血压。原发性高血压中常见。这类病变的肾脏兼有排钠障碍和肾素分泌增加,即一方面血容量增加,一方面小动脉收缩加强,两者均可导致血压升高。血压升高和血容量增加又可抑制肾素分泌,最后达到平衡,即肾素张素、醛固酮的分泌均在正常范围之内。在治疗上需联合应用利尿排钠剂和抗肾素的药物。
